こんにちは!個別指導SUNS葛西校です。
みなさん、テスト結果がすべて返ってきたと思いますが、どうでしたでしょうか?
今回のテスト結果、テストに対する勉強の仕方など振り返って、改善するきっかけとしましょう!
前回は数学のテストの分析をしましたが、今回は葛西第三中3年生の期末テストの理科を振り返っていきたいと思います。
2年生の3学期や3年生になってから、理科の点数を思うように取れない人増えてきたんじゃないでしょうか。
というのも、生物分野や地学分野というのは暗記がしっかりしていれば、得点は安定します。
一方で、化学分野や物理分野は暗記だけでは得点は安定しません。
たとえば、化学分野でいうと、「電解質はどうして電流が流れるのか」、「電解質の化学式の特徴はなにか」、「酸(アルカリ)の特徴は?」
などに対してそれぞれで暗記してませんか?
元素の種類は山ほどあり、その種類によって特徴もさまざまです。
そのため、ひとつひとつ暗記するときりがなく、かなりの時間と正確さが要求されます。
酸(アルカリ)に必ず含まれるイオンはなにか、電流が流れるのは何が存在するからなのか、電解質の化学式はなにか、それぞれしっかり理解すれば、ただ”点”で覚えていた知識も”線”としてさらに理解が深まると思います。
そのような視点も踏まえて振り返っていきましょう!

まず全体を見ていきますと、磁界・化学分野で75点、天体分野で25点でした。
磁界・化学分野は大問1⃣~8⃣、
天体分野は大問1⃣~4⃣でした。
数学と同じで問題数が多いように思いました。
配点の少ない天体分野からいきます。
試験前には、暗記が中心となるから教科書やSUNSでの授業で解いた演習問題をしっかり暗記すればすべて解けると生徒に伝えておりました。
想定通り基本問題が中心で、きちんと暗記していた生徒は実際に満点をとってきてくれました!
天体を含む地学分野は、都立入試においても理科の点数が安定する重要な分野です。
難しい化学や物理分野に時間を割きがちですが、
都立入試を受験するうえで、まずは天体のような暗記をしっかりすれば解ける分野は確実に正解できるようにしていきましょう!
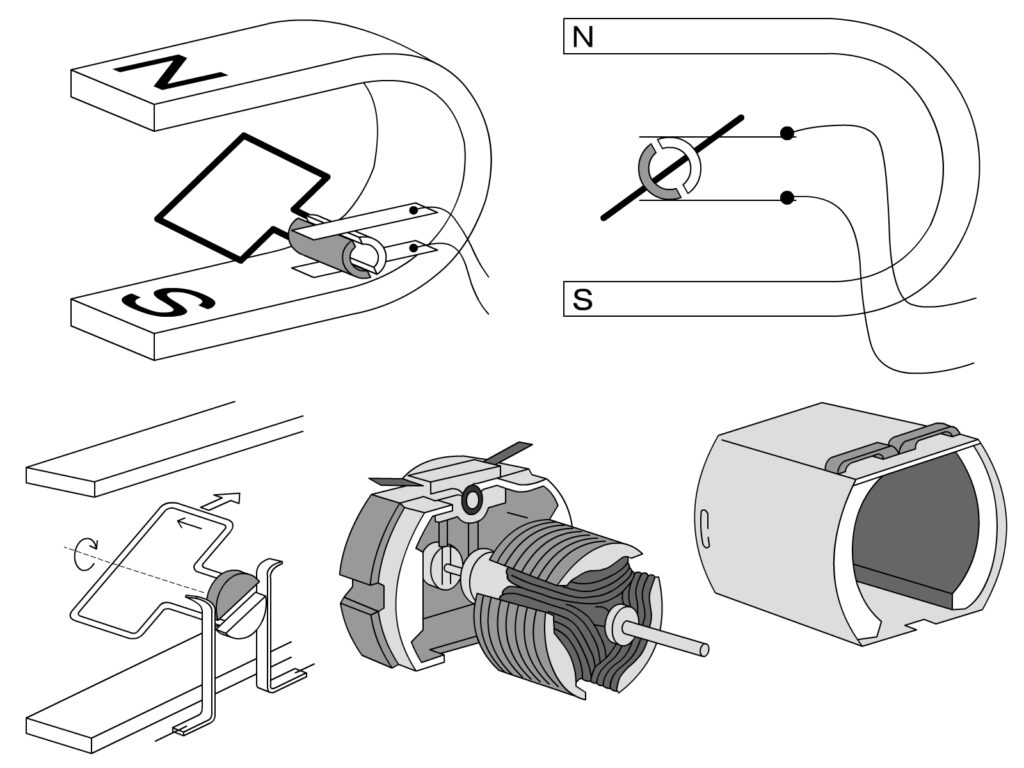
では、次に配点が大きかった磁界・化学分野にいきます!
まず大問1⃣~3⃣が磁界の問題でした。
大問1⃣はコイルに電流を流した際の磁界の問題でした。
教科書や演習教材に出てくる一般的な問題でした。ここは確実に取ってほしい問題です。
大問2⃣はモーターの問題。
問題としては決して難しくない一般的な、モーターの問題でした。
ただモーターの仕組みを試験前にきちんと理解している生徒は少ないと思います。
理屈が分かってしまえば、何も難しくはないですが、、、
今回できなかった人は、都立入試にも出題される可能性が十分にあるのでしっかり復習しましょう!
大問3は電磁誘導の問題でした。
この問題も基本問題中心で、最後の問題以外はできた人が多かったんじゃないかと思います。
しかし、最後の問題(下写真)はなかなか中学生に問うのはハードルが高かったかもしれません。

類題もあまり演習教材でも見たことがないので、もしかしたら学校の先生が授業中に説明されていたのかもしれません。
電磁誘導の範囲なので誘導電流が関与しているのは間違いないですが、
ここを解答できた人はしっかりと磁界の範囲を理解できていると自信を持っていいと思います。
ここまでが磁界の範囲でした(配点でいうと44点)。
基本問題が中心といえど、記述問題が6題出ているので最低30点は確保したい難易度でした。

では次!化学の範囲です。
大問4⃣~5⃣は、電解質を選ぶ選択問題やイオン式を問う問題です。
これはいずれも超基本問題の暗記問題です、落としてはいけない問題です。イオン式は試験前に絶対覚えとかなければいけません。
大問6⃣~7⃣は、塩化銅水溶液、塩酸の電気分解の問題でした。
中学3年生の化学の電気分解で出題されるのはこの2つだけといっても過言ではありません!
演習教材でも何度もSUNSの生徒には解いてもらっていたので、できていてほしい問題でした。
ただ電離式や化学式、イオン反応式など答え方がさまざまだったので、ここでミスした人もいるかもしれません。ケアレスミスした人は試験のときにしっかり見直しの時間を作るようにしましょう!
また、化学反応式もたくさん出題されていましたが、
当塾でもよく感じるのが、多くの生徒が化学(イオン)反応式についてきちんと理解できている人が少ないです。
せっかくなので、化学反応式について解説していきたいと思います。
たとえば、「塩酸の電気分解の化学反応式を書きなさい。」という問題があったとします。
(解) 2HCl→H2+Cl2
これ暗記している人いませんか?暗記せずとも自分でこの式は作ることが出来ます。
まず、塩酸が電気分解されたら、塩酸はHClなので、水素と塩素ができるなと想像つきます。
このとき、下のような間違いをする人がいます。
(×)HCl→H+Cl
これ何が間違っているかわかりますか?
水素や塩素などは分子として存在しています。どういうことかというと、水素はH(原子)ではなく、H(原子)が2つ結びついた分子(H2)として存在しています。そのため、化学反応式の右側は下のように書きます。
HCl→H2+Cl2
しかし、これではまだ未完成です。
化学反応式のルールとして、「矢印の左側と右側の元素の個数」を同じにしなければなりません。
この状態ですと、矢印の左側には水素が1個、塩素が1個、右側には水素が2個、塩素が2個です。
そこで、左側のHClを2個にすれば先ほどのルールに合うので
2HCl→H2+Cl2
が正解となります。
加えて、ここでしっかり理解しておいてほしいのが、HClの左側についている2は係数と呼ばれ、HClが2個あることを示します。すなわち、数学の文字式と考え方は同じです。
意外とみなさん、この考えが同じだと気付いていない人もいるので覚えておいてください。
これがわかってしまえば、化学反応式を読み解くと、
2つの塩酸から1つの水素と1つの塩素ができるということになります。
(高校生になると、この1つがmolという単位になります。)
今回の試験でも、「水素と塩素の発生量の比を答えなさい。」という問題がありましたが、化学反応式の意味を知っていれば、1:1と即答できたと思います。
最初に化学は暗記だけじゃだめといったのはこのようなところです。ただ化学反応式を暗記するのではなく、その式が何を表すか理解しましょう。
高校生になると、数えきれないくらいの化学反応式が出てきます。
暗記ではなく、化学反応式の作り方を理解し、そのような反応でも作れるようにならなければいけません。
では最後に大問8⃣です。
同じくイオンの問題でしたが、生徒にとっては初見問題かと思います。
塩化ナトリウムをガスバーナーで加熱し液体にすることで、電気が通るようになるという実験問題でした。
(1)は化学反応式でしたが、先ほどの化学反応式の作り方が分かっていれば、塩化ナトリウムからナトリウムと塩素ができることが文章中からわかるので、
2NaCl→2Na+Cl2
となると思います。
間違えた人は暗記ではなく自分で化学反応式を考えながら作ってみてください。
(2)は水に溶かしていない塩化ナトリウムが加熱によってなぜ電気分解できるかの記述問題でした。
ここは間違えても仕方がないですが、電気が通る=イオンが自由に動ける状態ということを理解していけば、部分点はもらえる問題だったかと思います。
以上が化学分野です。
難しい範囲とはいえ、解くのが難しい問題は数問しかありませんでした。
ただ化学分野は暗記の種類も多い、暗記だけでなく現象の理解も大事、といったところで、
できている子とできていない子の差が大きく出たのではないでしょうか。
今回の理科の範囲をできた子は、とても自信を持っていいと思います。
普段の勉強から、暗記だけでなく、しっかり内容理解が出来ている証拠です。
一方で、できていなかった子は、暗記だけではだめなんだと思って、勉強の仕方を変えていきましょう。
どういう風に勉強したらいいかわからない、そもそも理解できない、といったことがありましたら、
わかりやすく絶対に教えますので、いつでもお問い合わせください!
夏休みが絶好の復習期間ですよ!!!





